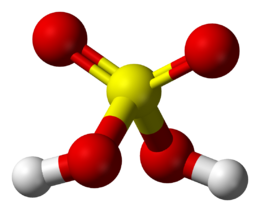
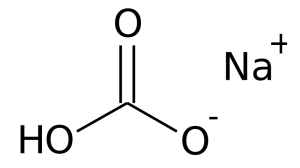
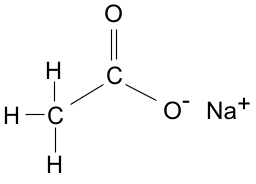
Perché il bicarbonato di sodio (NaHCO₃) pur essendo un sale acido rende basiche le sue soluzioni? - Quora
Perché il bicarbonato di sodio (NaHCO₃) pur essendo un sale acido rende basiche le sue soluzioni? - Quora

D7-1 La costante di dissociazione ionica dell'ammoniaca in acqua è uguale a 1.8·10-5. Determinare (a) il grado di dissociazione e (b) la concentrazione. - ppt scaricare