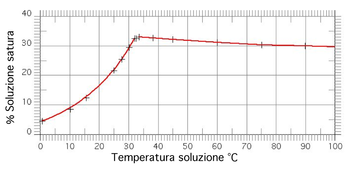
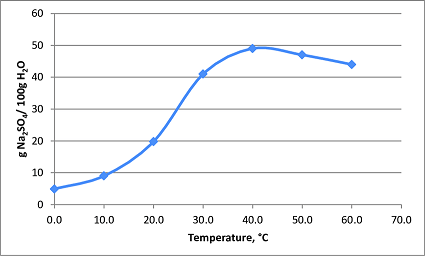
1a) Calcolare la solubilità in g/L del solfato di calcio in acqua deionizzata e in una soluzione di cloruro di calcio 0.50 M. (KPS del solfato di calcio: - ppt video online

Esercizi di chimica - Prodotto di solubilità Un tubo ricoperto da cromato di argento (Ag 2 CrO 4 ) è - StuDocu
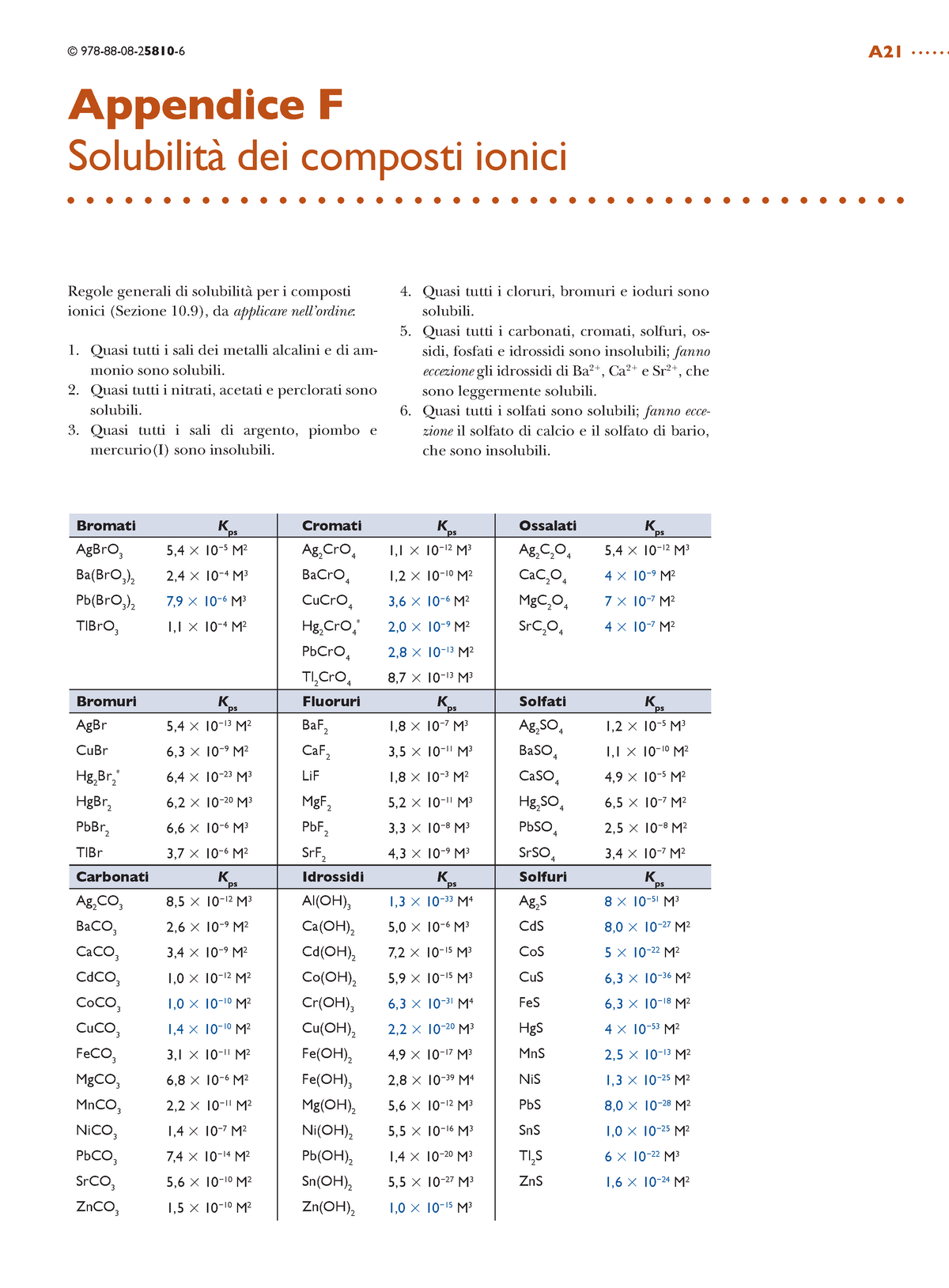
Prodotti di solubilità - Regole generali di solubilità per i composti ionici (Sezione 10), da - StuDocu

1a) Calcolare la solubilità in g/L del solfato di calcio in acqua deionizzata e in una soluzione di cloruro di calcio 0.50 M. (KPS del solfato di calcio: - ppt video online
Un manuale di diagnosi clinica mediante metodi microscopici e chimici, per studenti, medici ospedalieri e professionisti . Cristalli di solfato di calcio, (v. Jaksch.) sedimenti in soli due casi. In entrambe